
《评估和控制药物中DNA 反应性(致突变)杂质以限制潜在的致癌风险》(ICH HARMONISED GUIDELINE--ASSESSMENT AND CONTROL OF DNA REACTIVE (MUTAGENIC) IMPURITIES IN PHARMACEUTICALS TO LIMIT POTENTIAL CARCINOGENIC RISK-M7(R1)),于2013年2月发布,2017年5月获得ICH大会监管成员采纳并推荐ICH监管机构采纳。
该指南旨在提供一个可用于遗传毒性杂质的鉴别、分类、限定和控制的可行性框架,以限制潜在的致癌风险。意在补充ICH Q3A(R2)、Q3B(R2) 和M3(R2)支持开展人类临床试验和药品上市许可的非临床安全性研究。
遗传毒性杂质是指在较低水平时也有可能直接引起DNA损伤,导致DNA突变,可能引发癌症的DNA反应性物质,大部分为亲电试剂,如亚硝胺类物质。
1、遗传毒性杂质: Genotoxic impurities, GTI
2、潜在遗传毒性杂质: Potentially genotoxic impurities, PGI
根据ICH M7指南,遗传毒性杂质鉴别可采用两种方法:
1、通过数据库和文献检索致癌性和遗传毒性数据(致突变性)(CPDB,IRIS,NTP,ECHA等)。
2、使用(定量)结构活性关系(QSAR)进行计算。采用QSAR方法预测细菌突变试验(AMES)的结果来进行毒性评估。并采用两种QSAR预测方法:一个方法基于专家规则(expert rule-based),另一个方法基于统计学(statistical-based)。QSAR模型符合OECD导则。如果两种模型结果一致则认为结果可靠,如果结果不一致则需要提供支持数据进行专家分析。
根据文献数据库或者QSAR计算所得出的危害评估的结果,可将杂质分为5个类别,详细分类见下表。


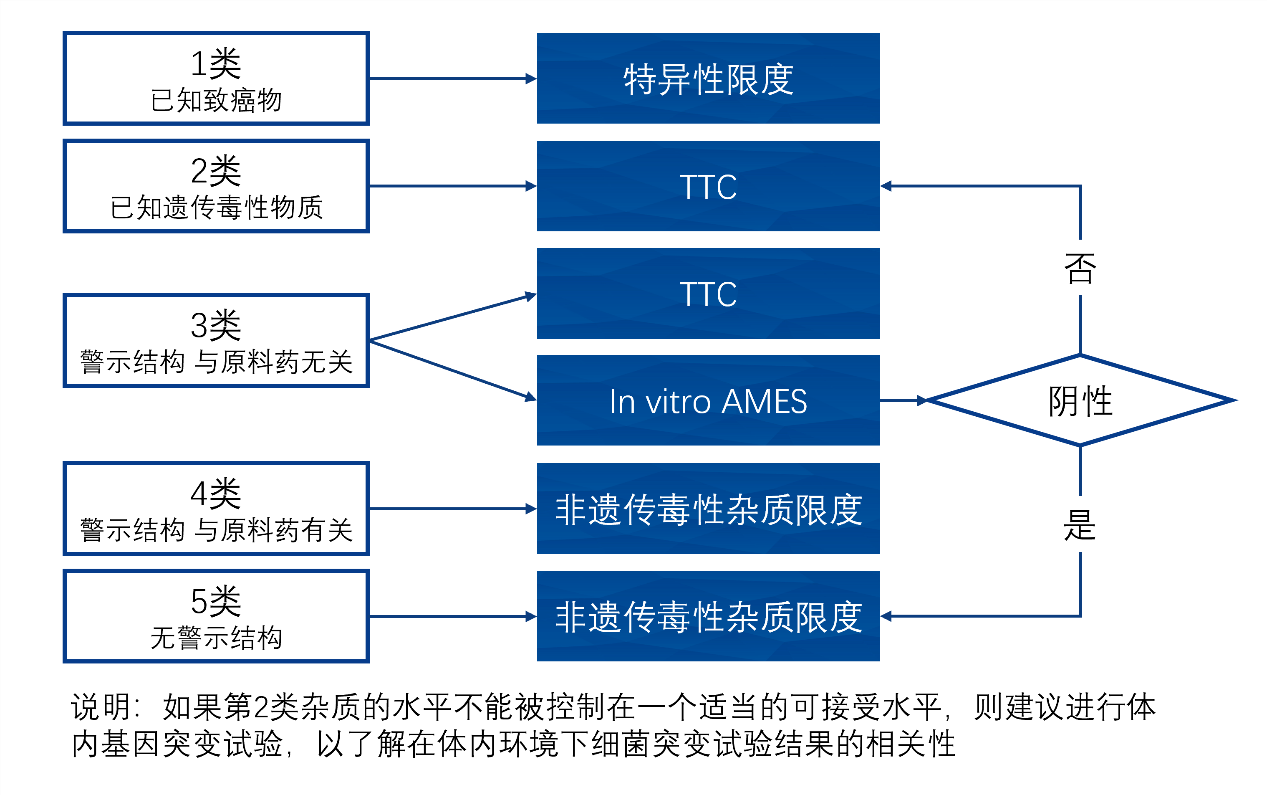
控制策略是一套基于对当前产品和对工艺的理解而制定的有计划的控制方法,用以保证工艺性能和产品质量。一个控制策略可以包括,但不限于以下内容:→点击咨询计算毒理
1、物料属性控制(包括原料、起始物料、中间体、试剂、溶剂、内包材);
2、设施和设备操作条件;
3、生产工艺设计中隐含的控制;
4、过程控制(包括过程检测和工艺参数);
5、原料药和制剂的控制(例如,放行检测)。
以勒标准在QSAR计算应用领域具有丰富的项目经验,已为医药企业的数十个产品提供遗传毒性杂质QSAR计算等服务,报告均成功应用于中国、美国、韩国等国家的药品注册并满足官方评审要求。

◆ ICH M7 杂质 QSAR预测报告
◆ 遗传毒性杂质TTC限量计算
◆ 遗传毒性杂质分类
◆ 相似物查询
◆ 亚硝胺类杂质分析
◆ AMES试验委托代理
※ 以勒申明:
本文内容来源:ECHA,由以勒标准翻译整理。以勒标准尊重知识产权,如转载内容涉及版权问题,烦请联系我们及时处理。翻译/整理不易,凡转载或引用本网站内容,请注明来源:杭州以勒标准,感谢您的支持!更多法规资讯实时跟踪,可搜索“以勒标准”官方微信公众号,获取第一手法规资讯,掌握最佳贸易时机!
< 上一个:无
> 下一个:专家文章 | QSAR在农药TE评估中的应用
0571-8519 0521
157875742
infor@jirehstandard.com